 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298K时,分别用金属Fe和Cd插人下述溶液中,组成电池。试判断何种金属首先被氧化?(1)溶液中含Fe2+和Cd2+的活度都是0.1。(2)溶液中含Fe2+的活度是0.1,而含Cd2+的活度是0.0036.
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“在298K时,分别用金属Fe和Cd插人下述溶液中,组成电池。试判断何种金属首先被氧化?(1)溶液中含Fe2+和Cd2+的活度都是0.1。(2)溶液中含Fe2+的活度是0.1,而含Cd2+的活度是0.0…”相关的问题
更多“在298K时,分别用金属Fe和Cd插人下述溶液中,组成电池。试判断何种金属首先被氧化?(1)溶液中含Fe2+和Cd2+的活度都是0.1。(2)溶液中含Fe2+的活度是0.1,而含Cd2+的活度是0.0…”相关的问题
第1题
A.电对Fe3+/Fe2+做正极
B.反应Fe+2Fe3+=3Fe2+的平衡常数大约为8×1040
C.电池组成式为(-)Fe|Fe2+(c1)||Fe2+(c2),Fe3+(c3)|Pt()
D.电池的标准电动势为0.331V
第2题
【题目描述】
第 56 题 盘亏的存货在处理时,应分情况记人下列账户() A.营业外收入
B.财务费用
C.管理费用
D.其他应收款
| 【我提交的答案】: AC |
| 【参考答案与解析】: 正确答案:CD |
略
【我的疑问】(如下,请求专家帮助解答)
请问 盘亏的存货在处理时,不是还有一项营业外支出吗?
第3题
第4题
在相同的气相色谱条件下,分别用N2和H2作流动相时,测得H-u曲线(Ⅰ,Ⅱ)如下:

看图试说明a'对应的H值为什么大于a点对应的H值?
第6题
A.构成原电池的正极和负极必须是两种不同的金属
B.Zn-Fe-HCl原电池中Fe为负极
C.在原电池中,电子流出的一极是负极,发生氧化反应
D.原电池放电时,电子是从负极流向正极
第8题
A.A.α减小时β也减小
B.B.α增大时β也增大,
C.C.α,β不能同时减小,减小其中一个时,另一个就会增大
D.D.A和B同时成立
E.E.α+β=1
第9题
若 298K 时反应N2O4 (g) = 2NO2(g) 的 Kө =0.1132,则当 N2O4 和 NO2 的分压均为1.0 kPa 时, 该反应()
A向生成 NO2 的方向进行
B向生成 N2O4 的方向进行
C正好达到化学平衡
D难于判断其进行方向
第10题
已知反应:

298K时的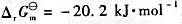 。试计算:
。试计算:
(1)该反应的标准平衡常数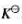 ;
;
(2)若空气中H2S的分压为3.1Pa,试计算可以确保铜单质免遭H2S腐蚀时H2的分压。