 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
应用附录中有关物资在25°C的标准摩尔生成焓的数据,计算下列反应在25°C时的ΔH及ΔU。
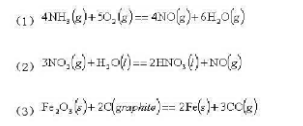
 答案
答案
查看答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
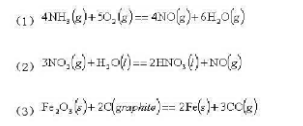
 答案
答案
 更多“应用附录中有关物资在25°C的标准摩尔生成焓的数据,计算下列反应在25°C时的ΔH及ΔU。”相关的问题
更多“应用附录中有关物资在25°C的标准摩尔生成焓的数据,计算下列反应在25°C时的ΔH及ΔU。”相关的问题
第1题
在25℃下,CaCl(s)溶解于水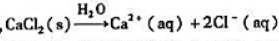 该溶解过程是自发的.计算其标准摩尔熵[变];其环境的煽变化如何?其值比系统的
该溶解过程是自发的.计算其标准摩尔熵[变];其环境的煽变化如何?其值比系统的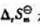 是大还是小?
是大还是小?
第2题
已知25℃时,液态水的标准摩尔生成吉布斯函数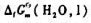 =-237.129kJ·mol-1,饱和蒸气压p''=3.1663kPa.求25℃时水蒸气的标准摩尔生成吉布斯函数.
=-237.129kJ·mol-1,饱和蒸气压p''=3.1663kPa.求25℃时水蒸气的标准摩尔生成吉布斯函数.
第4题
植物在光合作用中合成葡萄糖的反应可以近似表示为:
6CO2(g)+6H2O(1)=C6H12O6(s)+6O2(g)
计算反应的标准摩尔吉布斯自由能,判断反应在298K及标准状态下能否自发进行,已知葡萄糖的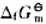 (C6H12O6·s) =-910.5kJ·mol-1。
(C6H12O6·s) =-910.5kJ·mol-1。
第7题
A.1、50、20
B.1.5、50、25
C.1.5、100、20
D.1.5、100、25
第9题
2
(g)达到平衡.此时,向反应系统中加入一定量的惰性组分H2O(g),则标准平衡常数Kθ(),C6H5C2H5(g)的平衡转化率α(),C6H5C2H3(g)的摩尔分数y(C6H5C2H3)().(选择填入:增大、减小、不变.)
第11题
(I)的标准摩尔生成焓分别为-394kJ·mol-1和-286kJ·mol-1计算C2H5OH(1)在298.15K时的标准摩尔生成焓。