 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某化学兴趣小组利用如图装置制取氨气,A中烧瓶内试剂可选用()
A.生石灰
B.生石膏
C.石灰石
D.氯化钙
 答案
答案
A、生石灰
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.生石灰
B.生石膏
C.石灰石
D.氯化钙
 答案
答案
A、生石灰
 更多“某化学兴趣小组利用如图装置制取氨气,A中烧瓶内试剂可选用()”相关的问题
更多“某化学兴趣小组利用如图装置制取氨气,A中烧瓶内试剂可选用()”相关的问题
第1题
工业上以氨气为原料制备硝酸的过程如下: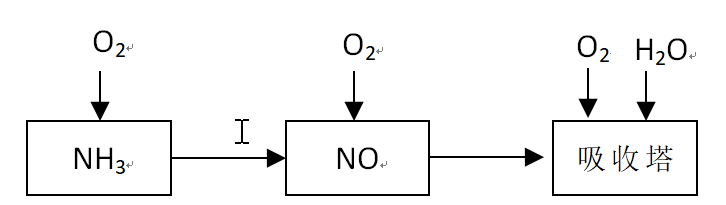 某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。
某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。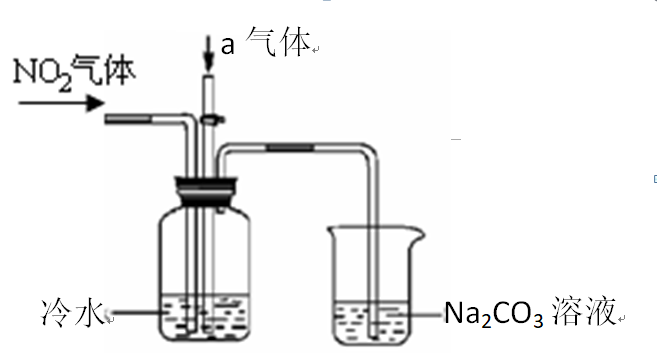
问题一、工业上用氨气制取NO的化学方程式是()。
问题二、连接好该装置后,首先进行的操作是()。
问题三、通入a气体的目的是()。
问题四、盛有Na2CO3溶液的烧杯为尾气处理装置,该装置中反应的化学反应方程式是2NO2+Na2CO3==NaNO2+()+()
问题五、已知:温度低于21.15℃时,NO2几乎全部转变为N2O4.工业上可用N2O4与水反应来提高硝酸产率。N2O4与a气体在冷水中生成硝酸的化学方程式是()。
问题六、一定条件下,某密闭容器中N2O4和NO2的混合气体到达平衡时,c(NO2)=0.50mol/L、c(N2O4)=0.125mol/L。则2NO2(g) N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。
N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。
第3题
【题目描述】
第 1 题在实验室制取氧气时,取MnO2和KClO3的固体混合物15.25g,加热至不再产生气体为止,收集到一定质量的氧气。某化学兴趣小组欲求得所制氧气的质量,他们将加热后剩余物冷却到一定温度后,通过多次加水测定剩余物质量的办法即可求出。加水的质量与剩余固体的质量见下表:(MnO2是不溶于水的固体粉末)
编号 | 1 | 2 | 3 | 4 |
| 加水的质量(g) | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 7.25 | 4.05 | m | 3 |
(2)所制得氧气的质量。
【我提交的答案】:
【参考答案分析】:
3 (由1和2可知加入10g水最多溶解3.2g KCl,而第三、第四次加水后溶解KCl为4.05g-3g﹤3.2g,则第三次加水后KCl完全溶解,剩余的固体全部是不溶于水的MnO2,则m=3,原混合物中KClO3为15.25g-3g=12.25g 。 ) (1分)
解:(2) 设可制得氧气的质量为x
2KClO32KCl + 3O2↑
245 96
15.25g-3g x (2分)
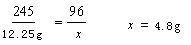
答:可制得氧气4.8克。 (2分)
【我的疑问】(如下,请求专家帮助解答)
由1和2可知加入10g水最多溶解3.2g KCl 为什么我需要在具体得思路 2KClO32KCl + 3O2↑
245 96
15.25g-3g x (2分) 看不懂
第5题
A.过滤和蒸馏是常用的净水方法,均可以使硬水变为软水
B.O2和CO2的组成中都含有氧元素,构成它们的微粒中都有氧分子
C.混合物是由不同物质组成的,同一种元素可能组成混合物
D.氧化物中都含有氧元素,所以含有氧元素的化合物一定是氧化物
第8题
A.正确,体现了面向全体学生的理念
B.错误,忽视了学生的个性差异
C.错误,忽视了培养学生的创新精神和实践能力
D.正确,体现了促进学生发展
第9题
某最小相位系统结构如图6-7(a)所示,G0(s)为受控对象的传递函数,图6-7(b)所示为该系统的开环对数幅频特性渐近线。试求:
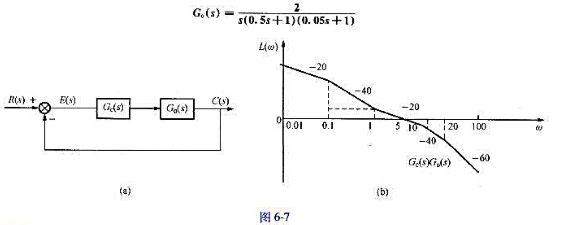
(1)写出开环传递函数;
(2)计算该控制系统的相角裕量;
(3)写出串联校正装置的传递函数Gc(s),说明是什么型式的校正。
第11题
【题目描述】
19.(12分)
某实验小组利用如下装置(部分固定装置略)制备氮化钙(Ca3N2),并探究其实验式。

(1)按图连接好实验装置。检查装置的气密性,方法是。
(2)反应过程中末端导管必须插入试管A的水中,目的是。
(3)制备氮化钙的操作步骤是:①打开活塞K并通入N2;②点燃酒精灯,进行反应;③反应结束后,;④拆除装置,取出产物。
(4)数据记录如下:

① 计算得到实验式CaxN2,其中x=.
② 若通入的N2中混有少量O2,请比较x与3的大小,并给出判断依据:。
【我提交的答案】:fghfd
【参考答案分析】:【答案】(1)关闭活塞,微热反应管,试管A中有气泡冒出,停止加热。冷却后若末端导管中水柱上升且高度保持不变,说明装置气密性良好。
(2)防止反应过程中空气进入反应管,便于观察N2的逆流
(3)熄灭酒精灯,待反应管冷却至室温,停止通入氮气,并关闭活塞。
(4)①2.80 ②产物中生成了CaO
【解析】(1)见答案;(2)要保证整个装置不能混入其他气体;(3)一定要使玻璃管冷却后再停止通入气流;(4)要确定X值必须求出钙和氮的原子个数比根据题目给的数据可做如下计算①m(Ca)=(15.08-14.80)g=0.28g,m(N)= (15.15-15.08)g=0.07g,则n(Ca):n(N)=0.28/40 :0.07/14=7:5,则x=14/5;②若通入的N2中混有少量O2,则产物中就有可能混有了CaO,而Ca3N2中钙的质量分数为81.08﹪,CaO中钙的质量分数为71.43﹪,所以产物中混有了CaO会导致钙的质量分数减小,x的值偏小。
【我的疑问】(如下,请求专家帮助解答)
U形管的作用